Сайт призначений виключно для фахівців охорони здоров'я в Україні
Menu
Close
ОРИГІНАЛЬНЕ ДОСЛІДЖЕННЯ NAXOS
Порівняльна безпека та ефективність оральних антикоагулянтів при неклапанній фібриляції передсердь
Дослідження NAXOS
Eric Van GanseID, MD, PhD; Nicolas Danchin, MD, PhD; Isabelle Mahé, MD, PhD; Olivier Hanon, MD, PhD; Flore Jacoud, MSc; Maëva Nolin, MSc; Faustine Dalon, MSc; Cinira Lefevre, PhD; François-Emery Cotté, PharmD, PhD; Sabrina Gollety, PharmD, PhD; Bruno Falissard, MD, PhD; Manon Belhassen, PhD; Ph. Gabriel Steg, MD
Завантажено з http://ahajournals.org 16 червня 2020 р.
ОБГРУНТУВАННЯ І ЦІЛЬ: Ефекти прямих оральних антикоагулянтів при неклапанній фібриляції передсердь слід оцінити при фактичних умовах застосування. Франція має майже універсальну систему повного медичного обслуговування населення та уніфіковану медичну інформаційну систему, що дозволяє провести великий аналіз популяційного масштабу. Дослідження NAXOS (Оцінка апіксабану при попередженні інсульту та системної емболії у пацієнтів із неклапанною фібриляцією передсердь) мало на меті порівняти безпеку, ефективність та смертність при прийомі апіксабану проти антагоністів вітаміну К (АВК), ривароксабану і дабігатрану у пацієнтів, які раніше не отримували лікування оральними антикоагулянтами при неклапанній фібриляції передсердь.
МЕТОДИ: Це обсерваційне дослідження, що використовує дані для сплати медичної допомоги Французької державної системи охорони здоров’я, яке включало всіх дорослих із неклапанною фібриляцією передсердь, які розпочали прийом оральних антикоагулянтів з 2014 р. по 2016 р. Нас цікавили такі результати, як великі кровотечі, що призводили до госпіталізації (безпека), інсульт та системні тромбоемболічні ускладнення (ефективність), а також смертність з усіх причин. Для порівняльного аналізу застосовувались чотири підходи: співставлення за мірою схильності (МС; 1:n); як аналіз чутливості, співставлення за високорозмірною МС; корекція на МС; і поправка на відомі спотворюючі фактори. Для кожного результату оцінювали сукупну частоту захворюваності, що враховує конкуруючі ризики смерті.
РЕЗУЛЬТАТИ: В цілому, був проаналізований 321 501 пацієнт, із яких, відповідно, 35,0%, 27,2%, 31,1% і 6,6% розпочали прийом АВК, апіксабану, ривароксабану і дабігатрану. Апіксабан був асоційований із нижчою МС-співставленим ризиком великої кровотечі у порівнянні із АВК (відношення ризиків [ВР], 0,43 [95% ДІ, 0,40–0,46]) і ривароксабаном (ВР, 0,67 [95% ДІ, 0,63–0,72]), проте не дабігатраном (ВР, 0,93 [95% ДІ, 0,81–1,08]). Апіксабан був асоційований із нижчим ризиком інсульту і системних тромбоемболічних ускладнень, у порівнянні із АВК (ВР, 0,60 [95% ДІ, 0,56–0,65]), проте не ривароксабаном (ВР, 1,05 [95% ДІ, 0,97–1,15]) або дабігатраном (ВР, 0,93 [95% ДІ, 0,78–1,11]). Смертність з усіх причин була нижчою для апіксабану проти АВК, але не нижчою проти ривароксабану або дабігатрану.
ВИСНОВКИ: Апіксабан був асоційований із кращою безпекою, ефективністю та нижчою смертністю, аніж АВК; він мав кращу безпеку за ривароксабан і однакову безпеку із дабігатраном; і однакову ефективність у порівнянні із ривароксабаном і дабігатраном. Ці обсерваційні дані свідчать про можливі важливі різниці у результатах при прийомі оральних антикоагулянтів прямої дії, які слід дослідити у рандомізованих дослідженнях.
Адреса для листування: Eric Van Ganse, MD, PhD, PELyon, 11 Rue Guillaume Paradin, 69008 Lyon, France. Email [email protected]
Цей рукопис було надіслано до Michael Brainin, MD, Dr (hon), для перегляду експертами, редакторського рішення та кінцевого рішення щодо публікації.
Додаткові дані доступні для цієї статті за адресою https://www.ahajournals.org/doi/suppl/10.1161/STROKEAHA.120.028825.
На сторінці 2074 наведено Джерела фінансування та Розкриття інформації.
© 2020 The Authors and Bristol Myers Squibb. Stroke публікується від імені Американської асоціації кардіології — American Heart Association, Inc., через Wolters Kluwer Health, Inc. Це стаття відкритого доступу, відповідно до умов Ліцензії Creative Commons Attribution Non-Commercial-NoDerivs, що дозволяє використання, дистрибуцію та відтворення на будь-яких носіях, за умови належного цитування оригінальної роботи, некомерційного використання і без внесення змін або поправок.
Stroke доступний за адресою www.ahajournals.org/journal/str
Ключові слова: антикоагулянт, фібриляція передсердь, дані для сплати медичної допомоги, ефективність, смертність, ривароксабан, безпека
Хоча антагоністи вітаміну К (АВК) високоефективні для попередження і лікування тромбоемболічних ускладнень, вони мають обмеження, пов’язані із взаємодією з їжею та лікарськими засобами. АВК також мають вузький терапевтичний діапазон, що вимагає частого моніторингу, і особливу проблему підвищеного ризику внутрішньочерепних кровотеч.1 Прямі оральні антикоагулянти (ПОАК) становлять альтернативу АВК і пригнічують коагуляцію через пряме та специфічне зв’язування із активним сайтом тромбіну (дабігатран) або фактору Ха (ривароксабан і апіксабан). Через широкий терапевтичний індекс, ПОАК можна застосовувати у фіксованих дозах без рутинного моніторингу коагуляції і вони обмежено взаємодіють із харчовими продуктами та лікарськими засобами.2 Рандомізовані дослідження, в цілому, встановили кращу безпеку і щонайменше однакову ефективність ПОАК і АВК у пацієнтів із неклапанною фібриляцією передсердь (НКФП).3
Дослідження ARISTOTLE (Апіксабан для зниження ризику виникнення інсульту та інших тромбоемболічних ускладнень при фібриляції передсердь), рандомізоване подвійне сліпе дослідження, порівнювало апіксабан і варфарин у пацієнтів із НКФП і ≥1 додатковими факторами ризику тромбоемболії.4 У цьому дослідженні апіксабан знижував виникнення інсульту/системної емболії, кровотечі та смертність у порівнянні із варфарином.4 На основі дослідження ARISTOTLE, французькі регуляторні органи (Health Authority and Transparency Committee) затвердили апіксабан для попередження інсульту і системної емболії у пацієнтів із НКФП і ≥1 фактором(-ами) ризику, проте поставили вимогою післяреєстраційне дослідження ефективності. Щоб задовольнити цю вимогу, дослідження NAXOS (Оцінка апіксабану при попередженні інсульту та системної емболії у пацієнтів із неклапанною фібриляцією передсердь) було сплановане для опису реального застосування апіксабану та інших оральних антикоагулянтів (ОАК), доступних у Франції (АВК, дабігатран і ривароксабан). Дослідження NAXOS мало на меті оцінити ризики великих кровотеч (безпека), інсульту та системних тромбоемболічних ускладнень (ефективність), а також смертності з усіх причин, порівнюючи апіксабан із іншими ОАК. За відсутності рандомізованих контрольованих прямих порівняльних досліджень ПОАК, обсерваційні дані високої якості можуть надати корисну інформацію про порівняльну ефективність ПОАК. Оскільки Франція має майже універсальну систему медичного обслуговування та уніфіковану державну систему медичних даних (що покриває більше 90% населення Франції, це приблизно 66 мільйонів осіб), дослідження NAXOS надало гарну можливість для великого популяційного аналізу порівняльної ефективності ОАК, що застосовуються у Франції при НКФП, із фокусом на апіксабан.
МЕТОДИ
Через свій приватний характер, ці дані доступні тільки дослідникам, уповноваженим Французькою державною системою охорони здоров’я (French National Health System).
Інформована згода пацієнтів у цьому дослідженні не вимагалась (не застосовується до анонімних баз даних для оплати медичної допомоги).
Дизайн дослідження і джерела даних
Це історичне популяційне когортне дослідження використовувало дані для оплати медичної допомоги Французької державної системи охорони здоров’я (Systeme National des Donnees de Sante [SNDS]), що містять анонімну індивідуальну інформацію про соціодемографічні характеристики, всі компенсовані нелікарняні витрати на медичні послуги (без відповідних медичних показань або результатів) і всі виписні епікризи.
SNDS не надає прямої інформації про клінічний анамнез, клінічні або параклінічні обстеження (тютюнопаління, артеріальний тиск, індекс маси тіла, тощо), біологічні результати або будь-яку інформацію про роздачу лікарських засобів під час перебування у лікарні (окрім дуже дорогих препаратів) та будь-які дані про причину смерті; проте у SNDS зафіксовані події, що становили інтерес у нашому дослідженні (інсульт, велика кровотеча, смерть). Ця база даних для оплати медичної допомоги у даний час охоплює >90% населення країни.5
Популяція дослідження складалась із усіх пацієнтів віком ≥18 років, що охоплювались SNDS, із ≥1 відшкодуваннями лікування ОАК (АВК, апіксабан, ривароксабан або дабігатран) із січня 2014 р. по грудень 2016 р. і які заново починали одне із досліджуваних лікувань ОАК, тобто, без прийому того ж ОАК протягом 24 місяців перед індексною датою (тобто, датою першої роздачі).6 Пацієнтів із фібриляцією передсердь, діагностованою протягом 24 місяців перед включенням, ідентифікували за допомогою валідованого алгоритму, що раніше використовувався Bouillon та співавт.7 у дослідженні NACORA. Другий алгоритм було розроблено для ідентифікації НКФП (на основі визначення Європейського товариства кардіології).8
Пацієнтів, що відповідали критеріям включення, розподіляли по 4 окремим субкогортам, залежно від того, чи вони отримували протягом періоду дослідження АВК, апіксабан, ривароксабан чи дабігатран.
Не включали у дослідження пацієнтів із кількома лікуваннями ОАК, багаторазовими дозами або кількома спеціалістами, що призначали лікарські засоби на індексну дату і пацієнтів, яких можливо лікували щодо показань, інших, аніж попередження інсульту при НКФП.
Обраних пацієнтів спостерігали протягом їхньої експозиції до досліджуваного антикоагулянтного лікування. Таким чином, кожного пацієнта вивчали від індексної дати до переходу на інше антикоагулянтне лікування, припинення лікування, останнього запису про здоров’я пацієнта (останній запис у базі даних до 6-місячного періоду без компенсованої допомоги, що міг означати еміграцію або перехід до будинку престарілих), смерті або закінчення періоду дослідження (тобто, 31 грудня 2016 р.), залежно від того, що наставало раніше. Пацієнтів цензорували при першому настанні однієї з цих подій. Інформацію/визначення про перехід на інше лікування, припинення лікування і лікарське забезпечення наведено у Додаткових матеріалах у Data Supplement.
Результати
Результатами, які нас цікавили, були безпека, визначена як ризик великих кровотеч, що призводили до госпіталізації та були ідентифіковані через основні лікарняні виписні епікризи; ефективність визначена як ризик інсульту або системної тромбоемболії, що ідентифікувалися через основні лікарняні виписні епікризи; та смертність з усіх причин, що ідентифікувалась через дані про смерть, зареєстровані у системі SNDS (Таблиця I у Data Supplement). Безпеку також досліджували, враховуючи 3 специфічні зони кровотеч. У пацієнтів із >1 зоною кровотеч на дату першої великої кровотечі, клінічно найбільш тяжка подія враховувалась у такому порядку пріоритету: внутрішньочерепна кровотеча, шлунково-кишкова кровотеча та інша кровотеча. Показники, що представляють інші показники результатів, було адаптовано на основі Friberg та співавт.9 і було валідовано Bouillon та співавт.7 у базі даних SNDS.
Статистичні методи
Для кожної когорти пацієнтів, раніше нелікованих ОАК, соціодемографічні характеристики та супутні захворювання описувались за допомогою дескриптивної статистики.
Основний аналіз порівняння апіксабану проти кожного іншого ОАК провели за допомогою співставлення міри схильності (МС). Для кожного порівняння між апіксабаном та іншими ОАК визначили три МС, за допомогою регресійної логістичної моделі, що включала такі перемінні: соціодемографічні характеристики, спеціальність медичного працівника, що розпочав лікування ОАК, супутні стани, бал CHA2DS2-VASc, модифікований бал HAS-BLED, індекс коморбідності Чарлсона і лікарські засоби, що роздавалися протягом 3 місяців перед індексною датою. У випадку колінеарності колінеарні перемінні видаляли із МС. Провели декілька перевірок для забезпечення хорошого балансу МС і коваріат між апіксабаном та групами порівняння: спершу, розподіл МС у групах лікування проаналізували графічно. Потім перевірили баланс коваріат між групами лікування та порівняння за допомогою стандартизованої різниці.10 Пацієнтів з апіксабаном співставляли із пацієнтами, лікованими іншими антикоагулянтами за допомогою співставлення послідовного попарного найближчого сусіда 1:n (n перемінна і n≤3) без заміни, за допомогою логіт-перетворення МС і специфікованого допуску калібру 0,2 для SD для логіт МС.11 Якість співставлення перевіряли за допомогою абсолютних зважених стандартизованих різниць демографічних та клінічних коваріат (стандартизовані різниці <0,1 вказували на належний баланс між групами лікування).11
Після співставлення МС ризик кожного результату порівнювали між апіксабаном та кожним із інших ОАК за допомогою моделі пропорційних ризиків Кокса із робастною оцінкою дисперсії для врахування співставлення. Для врахування конкуруючого ризику смертності (оскільки смертність була >10% у когорті АВК), застосовували моделі Файна і Грея для порівняння результатів безпеки та ефективності між апіксабаном та АВК. Припущення про пропорційність перевіряли на експозицію шляхом включення взаємодії між часовою функцією та експозицією. Якщо припущення про пропорційність порушувалось, тоді обраховували 2 моделі: перша без урахування непропорційності, що обчислювала середній відносний ризик (ВР) для кожної експозиції протягом цього періоду і друга зі включенням взаємодії між часовою функцією (лог) та експозицією для ідентифікації потенційних змін ВР із часом.
Для підтримки робастності основного аналізу провели 3 додаткові аналізи (див. Додаткові матеріали у Data Supplement).
Всі статистичні аналізи проводили із використанням SAS (SAS Institute, NC), версія 9.4.
Аналіз чутливості
Аналіз чутливості провели, застосовуючи модифіковані визначення результатів: для результату безпеки, із доданням супутніх діагнозів при перебуванні у лікарні при великих кровотечах і доданням трансфузії (через коди медичних процедур); і для результату ефективності, із виключенням діагнозу геморагічного інсульту. Порівняння між апіксабаном та кожним із інших ОАК проводили за тим самим методом, що і при основному аналізі.
Етика
Це дослідження було затверджене Французьким інститутом даних охорони здоров’я (Institut National des Donnees de Sante, затвердження № 136, датоване 8 вересня 2015 р). Дослідження було проведене із використанням анонімних даних, затверджене Державним комітетом з інформатики та свобод громадян (Commission Nationale Informatique et Libertes, затвердження № 1877931 датоване 17 березня 2016 р.) і зареєстроване на URL: https://www.clinicaltrials.gov; Унікальний ідентифікатор: NCT02640222.
Ідентифікація популяції дослідження
Серед 1 951 218 пацієнтів, включених до Французької державної бази даних охорони здоров’я, які отримали ≥1 курсів АВК, апіксабану, ривароксабану або дабігатрану з 2014 по 2016 рр., 1 040 864 пацієнта (53,3%) розпочали одне із досліджуваних лікувань ОАК. Майже всі пацієнти (99,8%) були віком ≥18 років на дату початку прийому ОАК, 438 280 пацієнтів мали фібриляцію передсердь і 93,9% (411 700 пацієнтів) мали НКФП. Після виключення пацієнтів без валідної інформації про дозування або спеціаліста, що призначав лікування, 411 077 пацієнтів було включено до популяції дослідження.
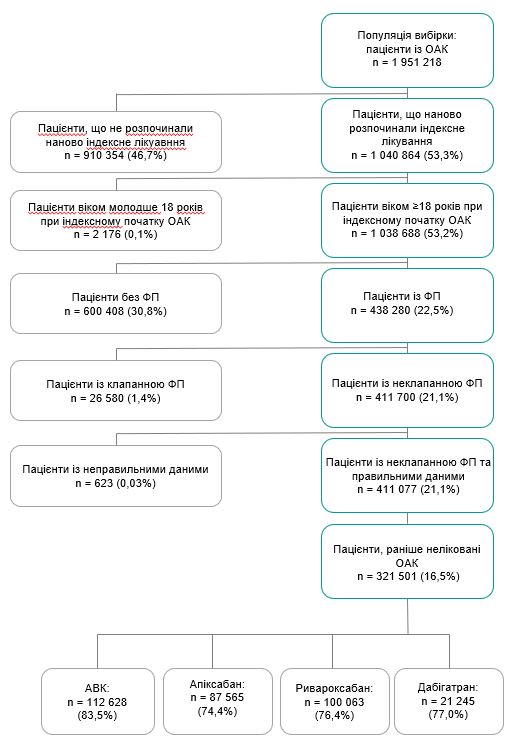
Із цих включених, було ідентифіковано 321 501 пацієнта із НКФП, раніше нелікованих ОАК: 112 628 (35,0%) розпочали прийом АВК (69,8% приймали флуіндіон, 27,3% приймали варфарин і 2,9% приймали аценокумарол), в той час як 87 565 (27,2%), 100 063 (31,1%), і 21 245 пацієнтів (6,6%) розпочали прийом, відповідно, апіксабану, ривароксабану і дабігатрану (Рисунок 1).
Характеристики пацієнтів
Попередньо узгоджені дані показали значні різниці у характеристиках пацієнтів між когортами, що розпочали прийом АВК, апіксабану, ривароксабану і дабігатрану (Таблиця). Пацієнти у когортах АВК були старші за віком, мали вищий ризик інсульту і більше супутніх станів, аніж пацієнти, що отримували ПОАК. Серед ПОАК пацієнтів, пацієнти із апіксабаном були старші за віком, мали вищий ризик інсульту і частіше мали супутні захворювання, аніж у когортах ривароксабану і дабігатрану.
Середня тривалість спостереження становила 316 днів (медіана = 218 днів) для пацієнтів, раніше нелікованих антикоагулянтами, що отримували АВК. Для тих, хто приймав апіксабан, ривароксабан і дабігатран, середня тривалість спостереження становила, відповідно, 286 (медіана = 213), 318 (медіана = 205) і 329 днів (медіана = 186).
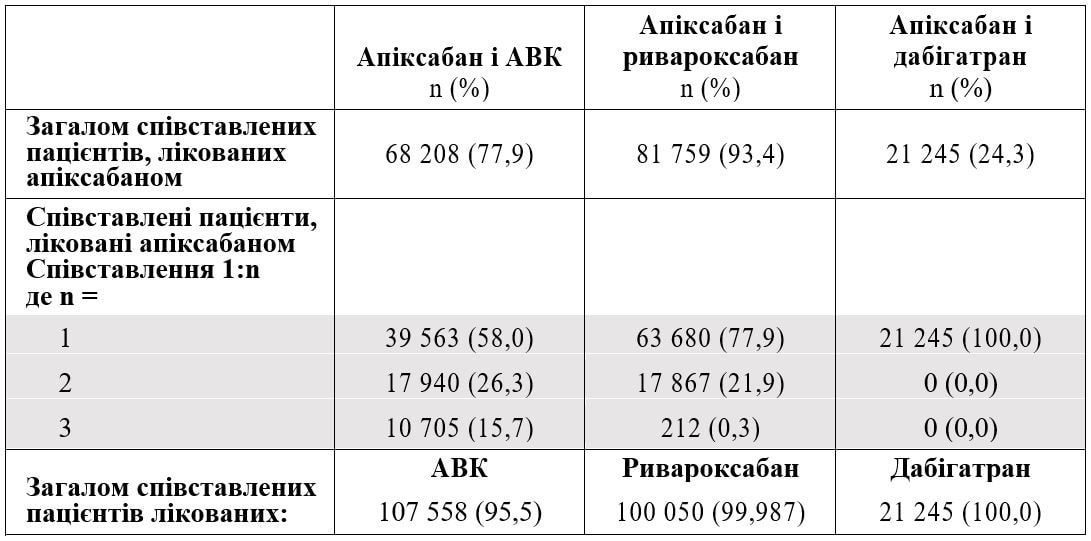
Серед пацієнтів, лікованих апіксабаном, 68 208 можна було співставити із 107 558 пацієнтами із АВК, 81 759 можна було співставити із 100 050 пацієнтами із ривароксабаном і 21 245 можна було співставити із 21 245 пацієнтами із дабігатраном (Таблиця II у Data Supplement).
Після співставлення за мірою схильності, абсолютні зважені стандартні відмінності для всіх спотворюючих факторів становили <10% (Рисунок I у Data Supplement). Спотворюючі фактори після зважування для кожної із співставлених когорт наведені у Таблиці III у Data Supplement.
Результати під час спостереження
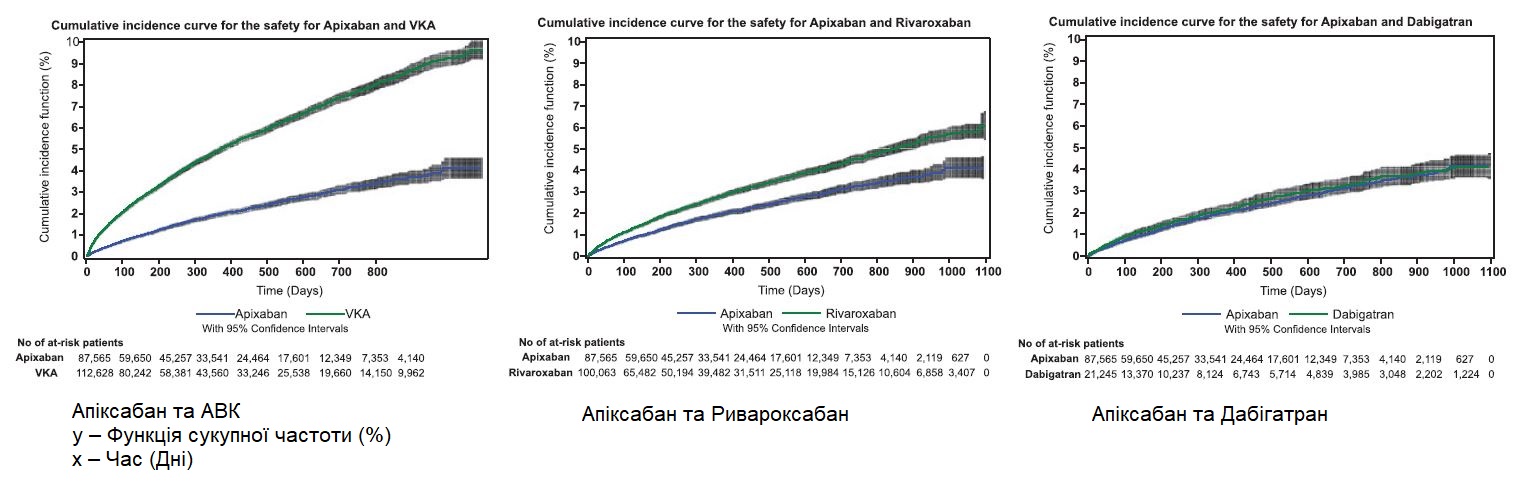
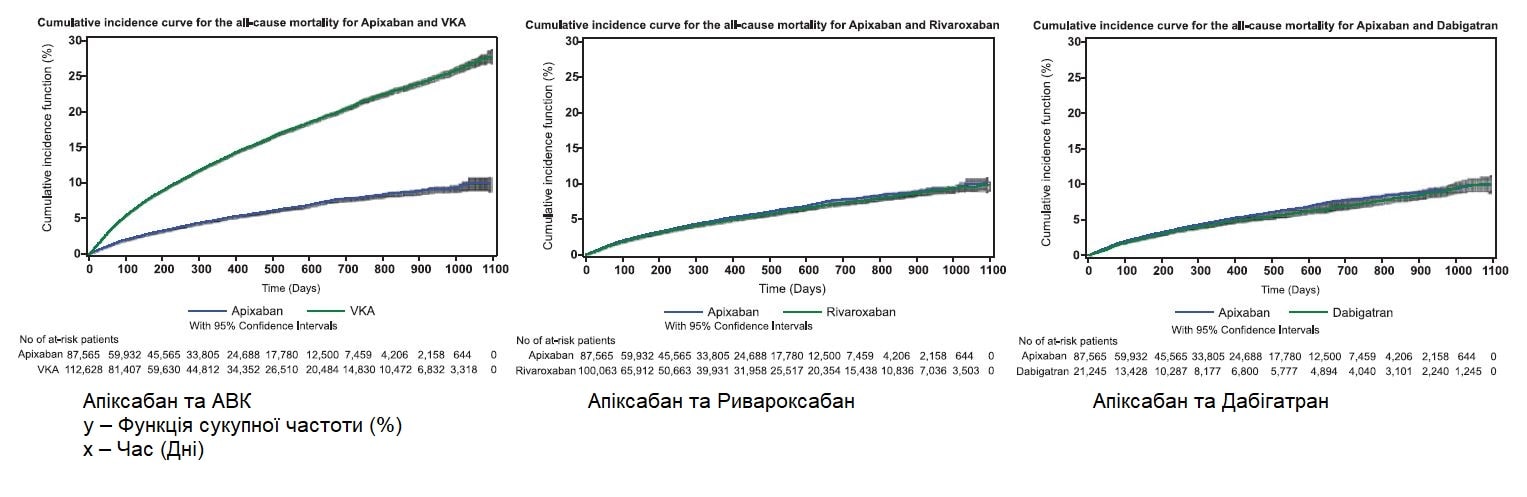
Сукупна частота великих кровотеч під час періоду спостереження, беручи до уваги конкуруючий ризик смерті у когорті АВК, становила 4,00% для апіксабану і 9,54% для АВК, 4,24% для апіксабану і 6,38% для ривароксабану і 3,80% для апіксабану і 4,31% для дабігатрану (Рисунок 2). Сукупна частота інсульту або системних тромбоемболічних ускладнень під час періоду спостереження, беручи до уваги конкуруючий ризик смерті у когорті АВК, становила 3,16% для апіксабану і 6,13% для АВК, 2,93% для апіксабану і 3,22% для ривароксабану і 2,56% для апіксабану і 3,28% для дабігатрану (Рисунок 3). Сукупна частота смертності з усіх причин під час періоду спостереження становила 11,10% для апіксабану і 26,55% для АВК, 9,18% для апіксабану і 9,66% для ривароксабану і 8,36% для апіксабану і 10,05% для дабігатрану (Рисунок 4).
Рисунок 1. Обрання популяції дослідження.
Процент пацієнтів, які розпочали прийом антагоністів вітаміну К (АВК), апіксабану, ривароксабану та дабігатрану наведено на основі кількості пацієнтів, раніше нелікованих оральними антикоагулянтами (n=321 501). ФП означає фібриляцію передсердь.
Порівняння результатів
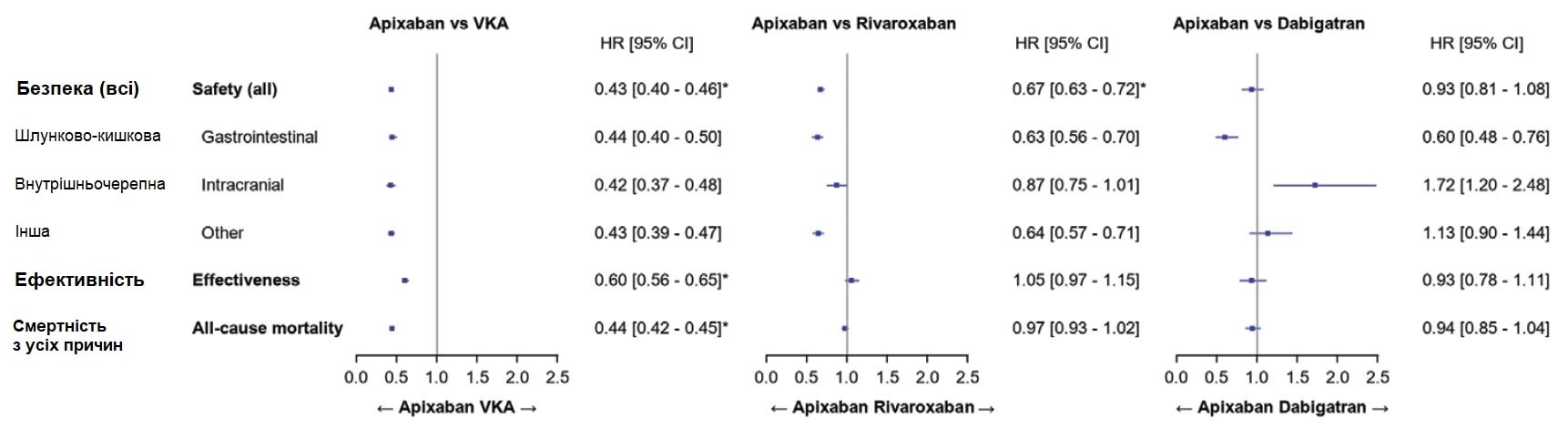
Після співставлення міри схильності пацієнти, що розпочинали прийом апіксабану, мали нижчий ризик великих кровотеч (всі великі кровотечі ВР, 0,43 [95% ДІ, 0,40–0,46]; шлунково-кишкові кровотечі ВР, 0,44 [95% ДІ, 0,40–0,50]; внутрішньочерепні кровотечі ВР, 0,42 [95% ДІ, 0,37–0,48]; та інші кровотечі ВР, 0,43 [95% ДІ, 0,39–0,47]) та інсульту і системних тромбоемболічних ускладнень (ВР, 0,60 [95% ДІ, 0,56–0,65]) та нижчий ризик смертності з усіх причин (ВР, 0,44 [95% ДІ, 0,42–0,45]), аніж співставлені пацієнти, що розпочинали прийом АВК (Рисунок 5). Пацієнти, ліковані апіксабаном, мали нижчий ризик великих кровотеч, аніж ліковані ривароксабаном (ВР, 0,67 [95% ДІ, 0,63–0,72]), хоча ризик інсульту та системних тромбоемболічних ускладнень (ВР, 1,05 [95% ДІ, 0,97–1,15) і ризик смертності з усіх причин (ВР, 0,97 [95% ДІ, 0,93–1,02]) були співставними (Рисунок 5). Пацієнти, ліковані апіксабаном, також показували нижчий ризик шлунково-кишкових кровотеч (ВР, 0,63 [95% ДІ, 0,56–0,70]) та інших кровотеч (ВР, 0,64 [95% ДІ, 0,57–0,71]), проте співставний ризик внутрішньочерепних кровотеч (ВР, 0,87 [95% ДІ, 0,75–1,01], аніж ліковані ривароксабаном. У порівнянні із пацієнтами, лікованими дабігатраном, пацієнти з апіксабаном мали співставний ризик великих кровотеч (ВР, 0,93 [95% ДІ, 0,81–1,08]), інсульту та системних тромбоемболічних ускладнень (ВР, 0,93 [95% ДІ, 0,78–1,11]) і смертності з усіх причин (ВР, 0,94 [95% ДІ, 0,85–1,04]) (Рисунок 5). Пацієнти з апіксабаном також мали нижчий ризик шлунково-кишкових кровотеч (ВР, 0,60 [95% ДІ, 0,48–0,76]), співставний ризик інших кровотеч (ВР, 1,13 [95% ДІ, 0,90–1,44]) і вищий ризик внутрішньочерепних кровотеч (ВР, 1,72 [95% ДІ, 1,20–2,48]), аніж ліковані дабігатраном. У випадку порушення припущення про пропорційність, напрямок асоціації не модифікували після включення взаємодії між часовою функцією та експозицією.
Результати додаткових аналізів, із поправкою на спотворюючі фактори, поправкою на МС та співставлення за високорозмірною мірою схильності, здебільшого відповідали результатам основного аналізу, як показано на Рисунку ІІ у Data Supplement. Результати аналізу чутливості із застосуванням модифікованих визначень результату (безпека та ефективність) також, загалом, відповідали основному аналізу (Рисунок III у Data Supplement).
Таблиця. Попередньо співставлені вихідні демографічні та клінічні характеристики у пацієнтів за 24 місяці до індексної дати лікування ОАК у когортах, раніше нелікованих ОАК
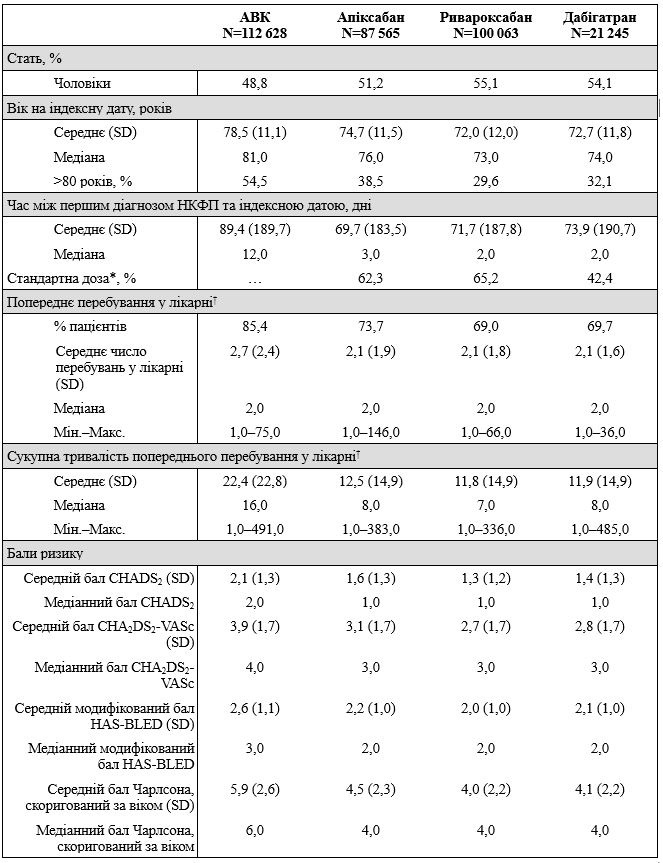
*Стандартні дози: апіксабан 5 мг двічі на добу, ривароксабан 20 мг один раз на добу і дабігатран 150 мг двічі на добу.
†У пацієнтів із пост-стаціонарним лікуванням.
ОБГОВОРЕННЯ
Із загальною когортою 321 501 пацієнтів із НКФП, раніше нелікованих ОАК, NAXOS є одним із найбільших обсерваційних досліджень, що оцінювало прийом і ефекти ОАК, яке пропонує перспективу на основі популяції держави щодо застосування антикоагулянтів у повсякденному житті. У цьому дослідженні вибір антикоагулянта був чітко різним залежно від профілю пацієнта, при чому пацієнти, які розпочинали прийом ПОАК, мали нижчий профіль серцево-судинного ризику, аніж пацієнти, що розпочинали прийом АВК. Серед пацієнтів, яким призначали ПОАК, пацієнти із апіксабаном мали вищий серцево-судинний ризик, вищий бал CHA2DS2-VASc і більше супутніх станів (вищий бал Чарлсона) аніж серед пацієнтів, які отримували інші засоби. Після співставлення за МС, апіксабан був асоційований із кращою безпекою та ефективністю у порівнянні із АВК. Апіксабан також показав кращу безпеку проти ривароксабану, хоча ефективність 3 ПОАК була співставною. Ризик смертності з усіх причин був нижчий для апіксабану проти АВК, хоча він був співставним для 3 ПОАК.
Для підтримки робастності основного аналізу і для включення всієї популяції (без систематичної похибки, пов’язаної із вибуванням учасників), ми провели 2 додаткових аналізи, застосовуючи корекцію на спотворюючі фактори і застосовуючи корекцію на МС. Більше того, намагаючись покращити класичну МС, ми провели третій додатковий аналіз, застосовуючи співставлення за високорозмірною мірою схильності. На додачу, для підтримки валідності визначень для результатів, ми провели аналіз чутливості, застосовуючи модифіковані визначення цих результатів. В цілому, цей додатковий аналіз чутливості дав результати, що відповідали результатам основного аналізу.
Рисунок 2. Криві сукупної частоти для оцінки великих кровотеч, що призводили до госпіталізації (безпека) протягом всього періоду спостереження.
АВК – антагоніст вітаміну К.
Ідентифікацію пацієнтів із НКФП та асоційованими балами ризику на основі баз даних для оплати медичної допомоги провести складно.12 Алгоритм, що використовувався у NAXOS, базувався на критеріях, раніше використаних у дослідженнях ARISTOTLE4 і NACORA (Nouveaux Anticoagulants Oraux et Risques Associes).7 Стосовно соціодемографічних та клінічних даних, пацієнти, включені у дослідження NAXOS були співставлювані із пацієнтами від 3 попередніх великих французьких обсерваційних досліджень,7,13,14 у яких пацієнти, ліковані АВК, були старшими за пацієнтів, лікованих ПОАК. Вік та супутні захворювання пацієнтів, включених у дослідження NAXOS, були аналогічні пацієнтам у дослідженні PAROS (Апіксабан у пацієнтів із фібриляцією передсердь в умовах реального життя: крос-секційне дослідження у Франції), недавньому французькому крос-секційному дослідженні призначень ОАК у пацієнтів із НКФП.15
Спостереження безпеки, ефективності та смертності з усіх причин для апіксабану та АВК у дослідженні NAXOS відповідали результатам дослідження ARISTOTLE.4 Проте смертність пацієнтів, лікованих АВК, у дослідженні NAXOS була вищою (13,39%) (дані не наведено), аніж у ARISTOTLE (3,94%), ймовірно через старший вік пацієнтів у когорті NAXOS і через суворий процес відбору для визначення критеріїв включення у рандомізованих дослідженнях. Як правило, пацієнти, що набираються в обсерваційні дослідження у рутинній клінічній практиці, показують тенденцію до значно вищого ризику негативних результатів, аніж пацієнти у клінічних дослідженнях.16–18
Рисунок 3. Криві сукупної частоти для оцінки ризику інсульту та системних тромбоемболічних ускладнень (ефективність) протягом всього періоду спостереження.
АВК – антагоніст вітаміну К.
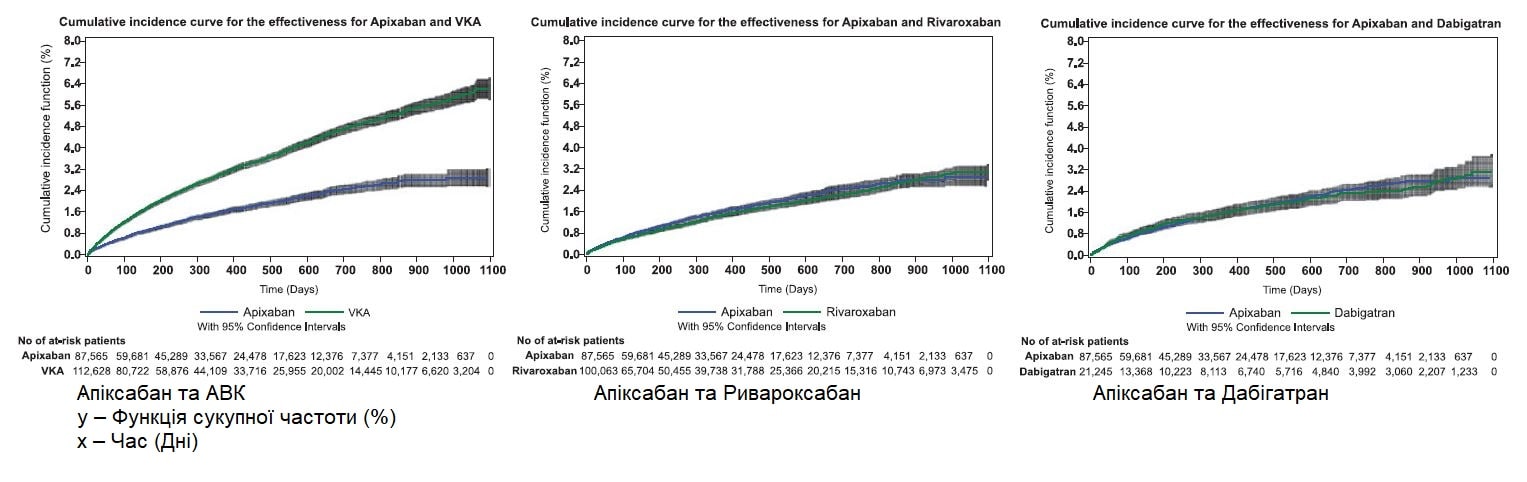
Рисунок 4. Криві сукупної частоти для оцінки смертності з усіх причин протягом всього періоду спостереження.
АВК – антагоніст вітаміну К.
Результати дослідження NAXOS відповідають результатам попередніх обсерваційних досліджень, як стосовно безпеки21,22 так і ефективності.22,23 У дослідженні проведеному Vinogradova та співавт.24 у Сполученому Королівстві, апіксабан був асоційований із нижчим ризиком кровотеч у порівнянні із АВК, проте не відмічали ніякої різниці для частоти виникнення ішемічного інсульту та смертності. У дослідженні зі США, апіксабан, проте не дабігатран або ривароксабан, був асоційований із нижчим ризиком інсульту/тромбоемболії у порівнянні з варфарином; всі 3 ПОАК були асоційовані зі зниженим ризиком внутрішньочерепних кровотеч, і як апіксабан, так і дабігатран були асоційовані зі зниженим ризиком великих кровотеч.22 У подальшому дослідженні у Сполучених Штатах, що базувалось на даних для оплати медичної допомоги, як апіксабан, так і дабігатран були асоційовані зі зниженим ризиком великих кровотеч у порівнянні із варфарином, в той час, як ривароксабан мав однаковий ризик.21 У данському дослідженні на основі даних для оплати медичної допомоги,25 всі 3 ПОАК були пов’язані зі зниженим ризиком внутрішньочерепних кровотеч у порівнянні із АВК, без різниці для інсульту або тромбоемболічних ускладнень. У нашому дослідженні, дабігатран був асоційований із значуще підвищеними ризиками шлунково-кишкових та інших кровотеч, проте зі значуще зниженим ризиком внутрішньочерепних кровотеч, у порівнянні із апіксабаном. Ці результати відповідали результатам дослідження Graham та співавт.26 У дослідженні зі США від Noseworthy та співавт.,27 апіксабан, ривароксабан і дабігатран мали однакову ефективність, хоча апіксабан показував нижчий ризик кровотеч, а ривароксабан мав підвищений ризик кровотеч; у іншому великому аналізі на основі населення США серед користувачів ПОАК, профілі користі-ризику апіксабану і дабігатрану були кращими за профіль ривароксабану.26
Хоча обсерваційні дослідження надали дещо суперечливі результати щодо смертності, безпеки і ефективності,24,28–31 дослідження NAXOS, як одне із найбільших, включає переважну більшість населення Франції і свідчить про потенційно клінічно значущі відмінності між ОАК, із можливим впливом на суспільну охорону здоров’я.
Рисунок 5. Форест-діаграми результатів основного аналізу (зі співставленими мірами схильності).
HR – відносний ризик; AVK – антагоніст вітаміну К.
У дослідженні ARISTOPHANES (Антикоагулянти для зниження ризику виникнення інсульту: обсерваційний сукупний аналіз наслідків для здоров’я та досвід пацієнтів) частота інсульту/системної емболії була нижчою і стандартні дози апіксабану і ривароксабану були аналогічні дозам варфарину, хоча ця частота була вищою для дабігатрану, аніж для варфарину.23 Ризик великих кровотеч був нижчий для апіксабану та дабігатрану, аніж для варфарину як при низьких, так і при стандартних дозах і ризик був вищим для ривароксабану при обох дозах. Як при низьких, так і при стандартних дозах ризик інсульту/системної емболії був нижчим для апіксабану, аніж для дабігатрану або ривароксабану, в той час як при низьких дозах цей ризик був вищим для дабігатрану, аніж для ривароксабану. Незалежно від дози, ризик великих кровотеч був нижчим для апіксабану та дабігатрану проти ривароксабану, що відповідало результатам NAXOS.23
Сильними сторонами дослідження NAXOS було те, що воно використовувало державну базу даних про оплату медичної допомоги (SNDS), що включала як первинну так і вторинну допомогу, надаючи широкий діапазон даних, включаючи соціодемографічну інформацію, основний медичний анамнез і вичерпні записи про відшкодування витрат на медичну допомогу, та включала >90% населення Франції. Це одна із найбільших державних обсерваційних когорт пацієнтів, які розпочинали прийом ОАК для лікування НКФП на сьогодні, даючи високу статистичну потужність. Результати підтвердили аналізи чутливості. Найбільш важливо те, що це дослідження популяційного масштабу, яке ґрунтувалося на базі даних єдиного платника (Французької державної системи охорони здоров’я), що мінімізувало потенціал систематичної похибки відбору. Нарешті, хоча неможливо виключити залишкову систематичну похибку на користь апіксабану у порівняннях, той факт, що серед пацієнтів, лікованих ПОАК, пацієнти із апіксабаном мали вищі бали CHA2DS2-VASc і бали Чарлсона, аніж пацієнти, що отримували інші ПОАК, свідчить, що залишкова систематична похибка при показаннях є малоймовірним поясненням кращої безпеки апіксабану і що ці результати є заниженими оцінками. Величина деяких розбіжностей між ПОАК свідчить, що є необхідність проведення прямих порівняльних рандомізованих клінічних досліджень. Згідго пробного підрахунку авторами на основі пропорції подій, буде необхідно приблизно 10 000 пацієнтів на групу лікування для оцінки результатів для різних ПОАК у гіпотетичному прямому порівняльному дослідженні (припускаючи 80% потужність).
Як і всі обсерваційні дослідження, NAXOS має обмеження: пацієнти із НКФП ідентифікувалися за алгоритмом, який міг виключити пацієнтів із менш тяжким захворюванням, таким як неускладнена пароксизмальна фібриляція передсердь. База даних SNDS не збирає інших діагнозів, окрім виписних епікризів; тому деякі фактори серцево-судинного ризику довелось ідентифікувати на показниках, що представляють інші показники на основі лікувань та лікарняних діагнозів (недоліки використання клініко-статистичних груп та нездатність повністю підтвердити природу/причину деяких результатів лікування добре відомі) і була відсутня інформація щодо значних спотворюючих факторів (кліренс креатиніну, гемоглобін, статус тютюнопаління, вага, дієта і споживання алкоголю), що часто зустрічається у даних про оплату медичної допомоги, або навіть у медичних записах, коли дані не оновлюються регулярно. Таким чином, бали CHADS2, CHA2DS2-VASc, модифікований бал HAS-BLED і бал Чарлсона, скориговані за віком, оцінювались за допомогою алгоритмів, що засновувались на показниках, що представляють інші показники. Було б цікаво відокремити етіологічні підтипи ішемічного інсульту та внутрішньомозкової кровотечі, оскільки ми розуміємо, що точна етіологія важлива для встановлення причинного зв’язку із застосуванням антикоагулянтів. Проте у цій базі даних ми не могли остаточно підтвердити природу/причину цих результатів лікування (наприклад, у деяких пацієнтів літнього віку не проводили радіологічного дослідження, коли загальний стан здоров’я був поганим).
Хоча ми вживали значних зусиль щоб мінімізувати спотворення, залишкове спотворення може бути присутнім, як і у всіх обсерваційних дослідженнях. Тим не менше, узгодженість (постійність) наших результатів висока, що свідчить про робастні докази. Було вироблено велику кількість моделей, що відкриває можливості корекції на множинну перевірку. Проте більшість наших результатів були високо статистично значущими і застосування поправок на множинне тестування не вплинуло б на критичні знахідки, навіть при застосуванні порогу P=0,001 і поправок Бонферроні. Нарешті, едоксабан не відшкодовується у Франції для лікування НКФП, а отже його не можна було включити у наш аналіз.
ВИСНОВКИ
У дослідженні NAXOS, пацієнти ліковані апіксабаном, мали нижчий ризик великих кровотеч, що призводять до госпіталізації, нижчий ризик інсульту та системних тромбоемболічних ускладнень і нижчий ризик смертності з усіх причин, у порівнянні із пацієнтами, що отримували АВК. Дослідження NAXOS також показало співставну ефективність всіх 3 ПОАК (апіксабану, ривароксабану і дабігатрану) із кращою безпекою апіксабану проти ривароксабану і без різниці у смертності між засобами. Враховуючи нестачу рандомізованих порівнянь між ПОАК, ці спостереження можуть становити інтерес для пацієнтів, клініцистів, регуляторних органів та страхових компаній/держави, що компенсують вартість медичних послуг.
ІНФОРМАЦІЯ ПРО СТАТТЮ
Отримано 8 листопада 2019 р.; остаточна редакція отримана 6 травня 2020 р; прийнято 12 травня 2020 р.
Частково представлено на Конгресі Європейського товариства кардіології (European Society of Cardiology), Париж, Франція, 31 серпня – 4 вересня 2019 р.
Приналежність до організацій
PELyon (Pharmaco Epidemiology Lyon), Ліон, Франція (E.V.G., F.J., M.N., F.D., M.B.).
Department of Respiratory Medicine, Croix Rousse University Hospital, Ліон, Франція (E.V.G.). HESPER (Health Services and Performance Research) 7425, University Claude Bernard Lyon 1, Ліон, Франція (E.V.G.). Hopital Europeen Georges Pompidou, Department of Cardiology, Париж, Франція (N.D.). Hopital Louis Mourier, AP-HP, Department of Internal Medicine, Коломб, Франція (I.M.). Universite de Paris, Department of Innovative Therapies in Haemostasis, INSERM, Париж, Франція (I.M.). Universite Paris Descartes, Sorbonne Paris Cite, Equipe d'accueil, 4468, Париж, Франція (O.H.). Hopital Broca, Department of Geriatrics, AP-HP, Париж, Франція (O.H.). Bristol-Myers Squibb, Рюей-Мальмезон, Франція (C.L., F.-E.C., S.G.).
INSERM U669, Париж, Франція (B.F.). Department of Cardiology, Hopital Bichat, AP-HP, Париж, Франція (P.G.S.). Universite de Paris, Париж, Франція (P.G.S.). INSERM U-1148, Париж, Франція (P.G.S.).
Подяки
Всі автори критично переглянули манускрипт. Drs Van Ganse і Steg забезпечили нагляд, започаткували і спланували дослідження, інтерпретували дані і склали робочий варіант манускрипту. Drs Danchin, Mahe, Hanon, і Falissard були членами Наукового комітету. F. Jacoud і M. Nolin провели статистичний аналіз. F. Dalon, Dr Lefevre, Dr Cotte, Dr Gollety, і Dr Belhassen зробили внесок у дизайн дослідження та інтерпретацію даних. Dr Van Ganse є гарантом дослідження. Ми дякуємо Georgii Filatov від Springer Nature, який провів редагування цього манускрипту англійською мовою.
Джерела фінансування
Цю роботу підтримали Bristol-Myers Squibb/Pfizer. Це дослідження було сплановане, проведене та написане дослідниками та науковою групою при PELyon. PELyon провів статистичні аналізи незалежно від спонсора.
Розкриття інтересів
Dr Van Ganse отримував персональні гонорари від PELyon, поза поданою роботою. Dr Danchin отримував персональні гонорари і нефінансову підтримку від BMS, персональні гонорари і нефінансову підтримку від Bayer, персональні гонорари і нефінансову підтримку від Pfizer протягом проведення цього дослідження, персональні гонорари і нефінансову підтримку від Amgen, персональні гонорари і нефінансову підтримку від AstraZeneca, персональні гонорари від Boehringer Ingelheim, персональні гонорари від Intercept, персональні гонорари від MSD, персональні гонорари від Servier, персональні гонорари від Sanofi та персональні гонорари від Novo Nordisk поза поданою роботою. Dr Mahe отримував гранти і персональні гонорари від BMS/Pfizer, під час проведення цього дослідження; персональні гонорари від Daiichi Sankyo, BMS, Pfizer і Bayer; та гранти і персональні гонорари від Leo Pharma, поза поданою роботою. Dr Hanon отримував персональні гонорари від Pfizer, персональні гонорари від BMS, гранти і персональні гонорари від Bayer, персональні гонорари від Boehringer, персональні гонорари від Boston Scientific, персональні гонорари від Leo Pharma і персональні гонорари від Aspen протягом проведення цього дослідження, персональні гонорари від Servier, персональні гонорари від AstraZeneca, персональні гонорари від Bouchara Recordati, персональні гонорари від Vifor, персональні гонорари від Novartis і персональні гонорари від HAC Pharma поза поданою роботою. F. Jacoud, M. Nolin, F. Dalon і Dr Belhassen є працівниками PELyon. Drs Lefevre, Cotte і Gollety є працівниками Bristol-Myers Squibb. Dr Falissard отримував персональні гонорари і нефінансову підтримку від BMS-Pfizer, протягом проведення цього дослідження; і персональні гонорари від Eli Lilly, BMS, Servier, Sanofi, GSK, HRA, Roche, Boehringer Ingelheim, Bayer, Almirall, Allergan, Stallergenes, Genzyme, Pierre Fabre, AstraZeneca, Novartis, Janssen, Astellas, Biotronik, Daiichi Sankyo, Gilead, MSD, Lundbeck, Actelion, UCB, Otsuka, Grunenthal і ViiV, поза поданою роботою. Dr Steg отримував персональні гонорари від BMS/Pfizer протягом проведення цього дослідження; гранти і персональні гонорари від Amarin; персональні гонорари від Amgen; гранти і персональні гонорари від Bayer; персональні гонорари від Boehringer Ingelheim; персональні гонорари від AstraZeneca; персональні гонорари від Idorsia; персональні гонорари від Novartis; персональні гонорари від Pfizer; гранти, персональні гонорари і нефінансову підтримку від Sanofi/Regeneron; і гранти і персональні гонорари від Servier поза поданою роботою; він також є винахідником патенту на застосування алірокумабу після гострого коронарного синдрому для зниження серцево-судинного ризику (всі авторські гонорари належать Sanofi).
Додаткові методи
Інформація/визначення переходу на інше лікування, припинення лікування і забезпечення лікарським засобом:
- Перехід на інше лікування визначався, як видача пацієнтам іншої антикоагулянтної молекули, зареєстрована після початку досліджуваного антикоагулянтного лікування. Дата переходу (та кінця спостереження) була датою першої видачі іншої антикоагулянтної молекули.
- Пацієнт вважався таким, що припинив лікування, якщо пройшло більше 30 діб після забезпечення останньої видачі антикоагулянтного лікування без його поповнення. Якщо протягом цього періоду мала місце госпіталізація, тривалість перебування у лікарні віднімалась від кількості днів без поповнення лікування. Для пацієнтів, які отримували лікування АВК (антагоністами вітаміну К), тестування Міжнародного нормалізованого відношення (МНВ) під час приватної госпіталізації враховувалось, як видача АВК. Тестування на МНВ використовувалось як заміна призначення АВК тільки з метою подовження експозиції до лікування АВК, проте воно не використовувалось як індексна дата (дата настання індексної події). Датою припинення лікування вважався останній день, що покривався останньою роздачею досліджуваного лікування НОАК (новим оральним антикоагулянтом).
- Забезпечення лікарським засобом НОАК визначалось на основі рекомендованої дози. Медіанна кількість днів забезпечення вираховувалась у групі пацієнтів АВК після екстракції даних, для пацієнтів із щонайменше двома роздачами лікування АВК (із однаковим кодом CIP) між 2014 р. та 2016 р.
Додаткові проведені коригувальні аналізи:
Застосовувались три додаткові порівняльні методи:
- За підходом модифікованої поправки: порівняння результатів із поправкою на спотворюючі фактори, застосовуючи алгоритм поетапного включення перемінних. Спершу, всі відомі та ідентифіковані спотворюючі фактори було включено в одномірну модель (модель Файна і Грея, або модель Кокса) для визначення значення p між коваріатою та результатом і для перевірки припущення про пропорційність. Всі спотворюючі фактори із значенням p<20% було включено у «повну модель», окрім коваріат, колінеарних із іншими спотворюючими факторами. Повною моделлю була багатофакторна модель, що включала всі спотворюючі фактори, значущі на рівні 20% в одномірній моделі, та наступні фактори, які були неповними: експозиція, вік на момент індексної дати, стать, тип спеціаліста, що призначив лікування і бали супутніх захворювань. Потім застосовувався ручний зворотній метод, тобто, поетапне усунення коваріат, не значущих статистично (для категоріальних перемінних, значення р пов’язане із включенням всіх модальностей перемінної у цю модель) на рівні 5% (від найбільшого до найменшого значення р). Спотворюючими факторами були статус вільного доступу до медичних послуг (коли 100% медичних витрат покривалися для осіб, чиї фінансові ресурси нижче порогового рівня), супутні стани через 24 місяці перед індексною датою і лікарські засоби, що видавалися протягом 3 місяців перед індексною датою. Робився вибір щодо збереження всіх перемінних, не дотримуючись припущення про пропорційність без модифікації моделі, перевіряючи, що включення у цю модель взаємодії між часовою функцією (лог) і перемінною не змінювало відношення між експозицією та результатом.
- Застосування підходу із поправкою на МС (міру схильності): порівняння результатів із корекцією на міру схильності. Ризик для ефективності, безпеки та смертності вивчався за допомогою того ж методу, що і для основного аналізу (модель Файна і Грея, або модель Кокса). Припущення про лог-лінійність перевірялось для МС і якщо припущення порушувалось, застосовувалась модель із МС, категоризованою у децилях. Якщо припущення про пропорційність порушувалось для МС, МС все ще залишали у моделі без будь-яких змін, після перевірки, що включення взаємодії між часом і МС не змінювало різко відношення між експозицією та результатом.
- Застосування методу співставлення даних Високорозмірної міри схильності (HdPS). Результати порівнювали за допомогою HdPS, намагаючись покращити здатність міри схильності через включення важливого числа спотворюючих факторів у бальну (скорингову) модель. Ці спотворюючі фактори були визначені у даних щодо оплати медичної допомоги завдяки алгоритму, розробленому Schneeweiss та співавт. Отже, на додачу до соціодемографічних коваріат, HdPS дозволяє врахувати історію стану здоров’я пацієнта протягом року до експозиції за допомогою таких вимірів:
- Амбулаторна роздача лікарських засобів,
- Закон про надання амбулаторної допомоги (коди CCAM),
- Амбулаторна біологія,
- Амбулаторні візити та консультації,
- Коди компенсацій для лікарів та діагностичні коди амбулаторій,
- Дані про виписку з лікарні для лікарняних діагностичних кодів,
- Дані про виписку з лікарні для лікарняних процедурних кодів.
Додаткові таблиці
Таблиця I. Діагнози, використані для ідентифікації інсульту та системних тромбоемболічних подій (результати ефективності) або великих кровотеч (результати безпеки).

АВК – антагоніст вітаміну К.
Таблиця III: Спотворюючі фактори для апіксабану і АВК, апіксабану і ривароксабану та апіксабану і дабігатрану - співставлення груп зі зважуванням
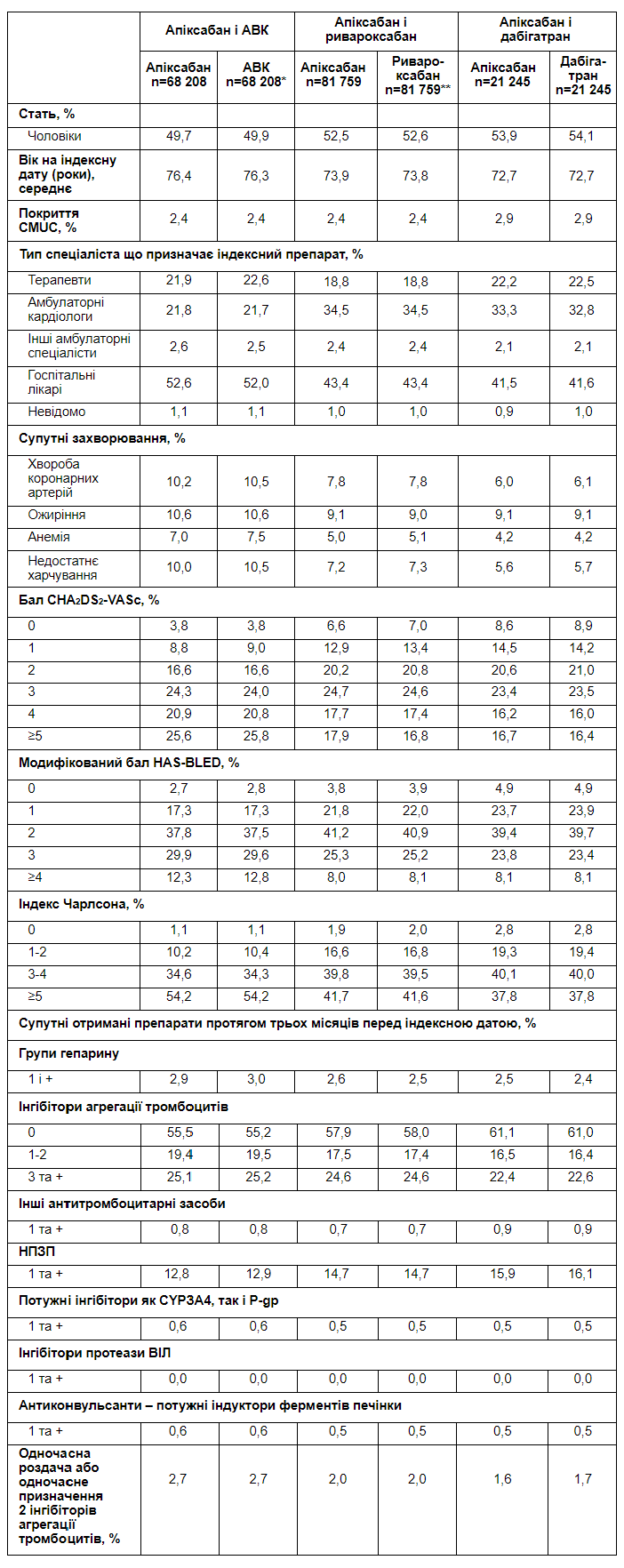
*Із 100 050 пацієнтів із ривароксабаном перераховані через співставлення 1:n, 63 680 пацієнтів з апіксабаном співставлені 1:1, 17 867 пацієнтів з апіксабаном співставлені 1:2 і 212 пацієнтів з апіксабаном співставлені 1:3
CHA2DS2-VASc, застійна серцева недостатність, гіпертензія, вік ≥75 років, цукровий діабет, попередній інсульт, транзиторний ішемічний напад або тромбоемболія, хвороба судин, вік 65–74 років, категорія статі;
CUMC, Couverture maladie universelle Protection Complémentaire; CYP, цитохром P450; ВІЛ, вірус імунодефіциту людини; P-gp, P-глікопротеїн; АВК, антагоніст вітаміну К.
Додаткові рисунки
Рисунок I: Баланс коваріат перед і після співставлення із застосуванням абсолютної зваженої стандартизованої різниці для когорт a) апіксабан і АВК, b) апіксабан і ривароксабан, і c) апіксабан і дабігатран
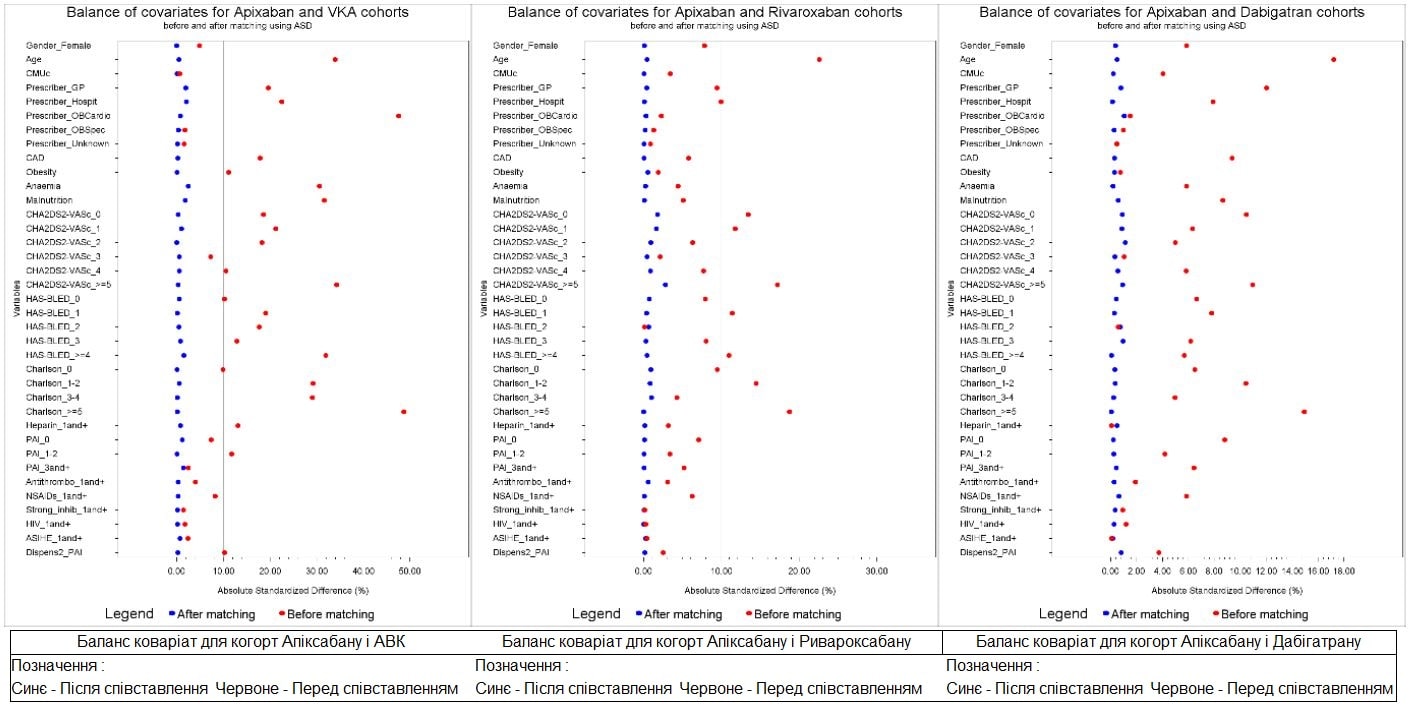
Рисунок II. Форест-діаграми для результатів основного (співставленого за МС) та додаткового (скоригованого на спотворюючі фактори, скоригованого на МС і співставленого за HdPS) аналізів
Для підтримки робастності основного порівняльного аналізу (тобто підходу співставлення МС), застосували три додаткові методи порівняння:
- Застосовуючи підхід модифікованої поправки: порівняння результатів із поправкою на спотворюючі фактори, застосовуючи алгоритм поетапного включення перемінних.
- Застосовуючи підхід, скоригований на МС: порівняння результатів, скоригованих за мірою схильності.
- Застосовуючи підхід даних Високорозмірної міри схильності (HdPS): результати порівнювали, використовуючи HDPS.
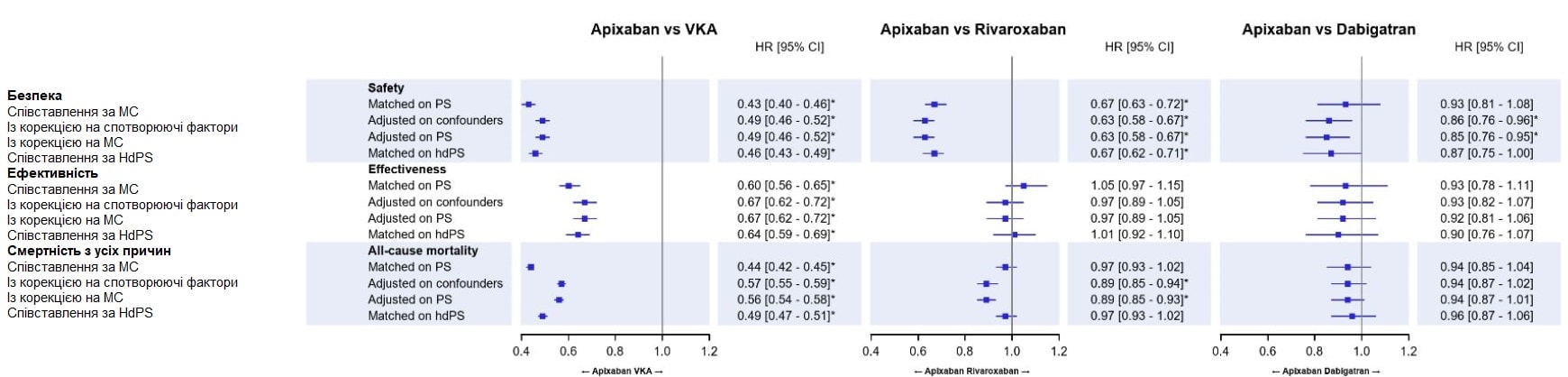
Безпека: великі кровотечі, що призвели до госпіталізації, та визначені на основі лікарняних виписних епікризів; ефективність: інсульт і системна тромбоемболія, визначені на основі лікарняних виписних епікризів.
Для порівняння між апіксабаном та АВК застосовували моделі Файна і Грея, оскільки смертність була високою у когорті АВК (>10%). Для інших порівнянь застосовували моделі Кокса.
У випадку порушення припущення про пропорційність, напрямок зв’язку не модифікували після включення взаємодії між часовою функцією та експозицією.
Рисунок III. Форест-діаграма результатів аналізу чутливості (порівняння співставлені за мірою схильності із модифікованими визначеннями результатів)
Для підтримки валідності визначень, що використовувались для ідентифікації результатів, провели аналіз чутливості із модифікованими визначеннями результатів:
- Розширення визначення результату безпеки до асоційованих діагнозів при госпіталізації та переливаннях крові.
- Видалення «геморагічного інсульту» із визначення подій ефективності (тобто, обмеження до «ішемічний інсульт, або не визначено» та «системні тромбоемболічні події»).
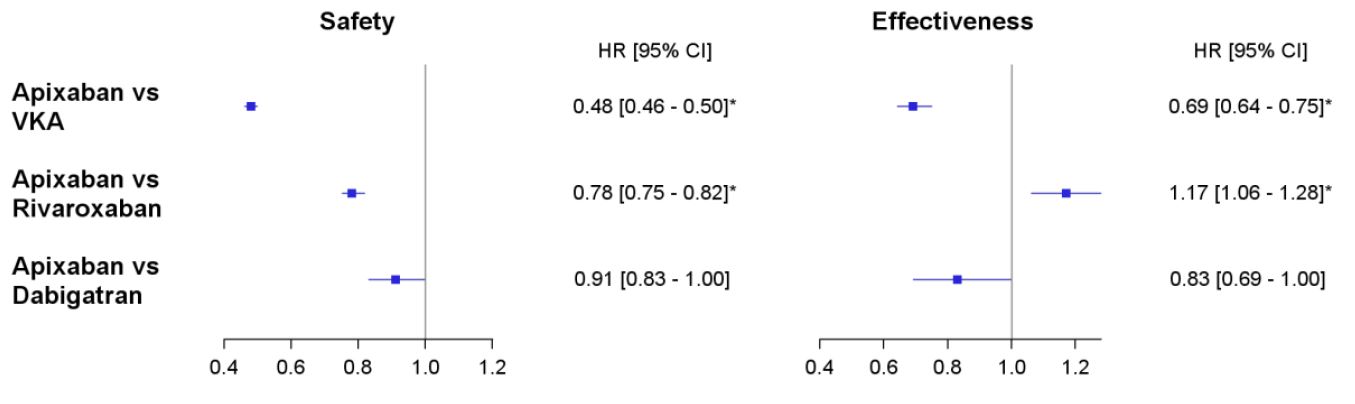
Safety – Безпека; Effectiveness – Ефективність; HR – Відносний ризик; CI – Довірчий інтервал
Безпека: як основні, так і асоційовані діагнози при перебуванні у лікарні з приводу великих кровотеч і переливань (на основі кодів медичних процедур); ефективність: основні діагнози при перебуванні у лікарні при інсульті та системних тромбоемболічних явищах (не враховуючи діагноз геморагічного інсульту).
У випадку порушення припущення про пропорційність, напрямок зв’язку не модифікували після включення взаємодії між часовою функцією та експозицією.
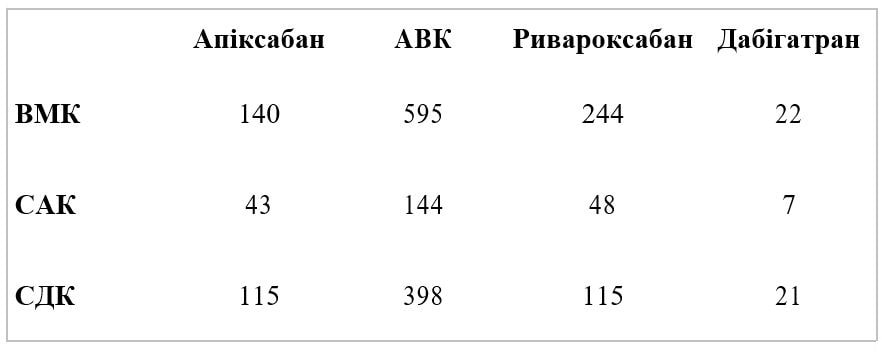
Ми спеціально не обчислювали ризики, пов’язані із різними зонами геморагічних інсультів (Внутрішньомозкова кровотеча (ВМК) проти Субарахноїдальної кровотечі (САК) проти Субдуральної кровотечі (СДК)), оскільки деякі цифри були дуже малими, як показує таблиця нижче і валідність детальних діагнозів спірна (наприклад, у деяких пацієнтів літнього віку не проводили радіологічного обстеження при загальному поганому стані здоров’я).
Клінічна інформація з Кардіології
- КАРДІОЛОГІЯ
- КЛІНІЧНА ІНФОРМАЦІЯ З КАРДІОЛОГІЇАналіз ефективності та безпеки оральних антикоагулянтів для тривалого лікування фібриляції передсердь у пацієнтів похилого вікуПрактичні аспекти антикоагулянтної терапії у різних категорій пацієнтівАнтитромботична терапія у пацієнтів із коморбідними станамиСтратегія вибору антикоагулянтної терапії у пацієнтів із неклапанною фібриляцією передсердьВидео: Фібриляція передсердь – типові симптомиОРИГІНАЛЬНЕ ДОСЛІДЖЕННЯ NAXOSВІДЕО: Як антикоагулянти можуть знизити ризик розвитку інсульту, що пов'язаний з фібриляцією передсердь?Профілактика інсульту при фібриляції передсердь: майстер-клас щодо ведення пацієнтаРанняя высокодозовая терапия аторвастатином после инфаркта миокарда с подъемом сегмента STВідео: Ви помічаєте ризикАртеріальна гіпертензіяДисліпідемія і серцево-судинні захворюванняАнтикоагулянтна терапія у пацієнтів із неклапанною фібриляцією передсердь: які інноваційні можливості ми маємо сьогодні?Ведення пацієнтів із неклапанною фібриляцією передсердь після перенесеного внутрішньочерепного крововиливу: тандем невролога та кардіологаАнтитромботична терапія у пацієнтів із неклапанною фібриляцією передсердь після перенесеного гострого коронарного синдрому та/або черезшкірного коронарного втручанняАнтитромботична терапія пацієнтів із неклапанною фібриляцією передсердь після перенесеного гострого коронарного синдрому та/або черезшкірного коронарного втручанняЕтнічність як суттєвий фактор ризику серцево-судинних захворюваньГіпертонія і серцево-судинні захворюванняЗахворювання периферичних артерій (ЗПА) і серцево-судинні захворюванняЦукровий діабет і серцево-судинне захворюванняГіпертрофія лівого шлуночка (ГЛШ) і серцево-судинні захворюванняСпосіб життя і серцево-судинні захворюванняВік як суттєвий фактор ризику серцево-судинних захворюваньАльбумінурія і серцево-судинні захворюванняХронічна ниркова недостатніть (ХНН) та серцево-судинні захворюванняХронічна серцева недостатність (ХСН) і серцево-судинні захворюванняСтенокардія + інфаркт міокарда (ІМ) та серцево-судинні захворюванняВідео про якість наших препаратівІшемічна хвороба серця
- Препарат «Еліквіс» (апіксабан) - №1 у світі серед інших нових пероральних антикоагулянтівПрограмма «Заради життя»Як запобігти до 80% серцево-судинних захворювань?Допомогти пацієнтам вийти із зони ризикуЕкспертна рада асоціації аритмологів УкраїниПродовжено проект з надання кардіологічної допомоги пацієнтам з порушенням коронарного кровообігуКорпоративний сайт компанії PfizerЕкспертна рада асоціації аритмологів УкраїниПро компанію PfizerПерсоніфікована антитромботична терапія як міждисциплінарна проблема
Слід повідомляти про небажані явища. Форми повідомлень та інформацію можна знайти за адресою https://aisf.dec.gov.ua/Account/LogOn
Для отримання доступу до інших матеріалів, ресурсів і отримання повідомлень про препарати та вакцини, які просуває Pfizer
Цей сайт призначений виключно для фахівців охорони здоров'я в Україні. Якщо ви є звичайним громадянином, який бажає отримати доступ до інформації про певний препарат, відвідайте http://www.drlz.com.ua
© Всі права захищено. Представництво "Пфайзер Експорт Бі.Ві" в Україні (2022)
"Цей сайт розроблений виключно для використання з професійною метою фахівцями охорони здоров’я в Україні.
Pfizer не гарантує відповідність інформації та сервісів сайту цілям і очікуванням Користувача, його безперебійну та безпомилкову роботу.
Користувач самостійно і за свій рахунок зобов’язується врегулювати всі претензії третіх осіб, пов’язані з діями Користувача при користуванні цим сайтом.
Користувач самостійно несе повну відповідальність за належне використання матеріалів, розміщених на сайті, в тому числі: за використання таких матеріалів у відповідності з вимогами законодавства України, за дотримання авторських прав і прав третіх осіб, а також, за дотримання положень цієї Угоди.
Підтвердіть: "
You are now leaving www.pfizerpro.co.uk. Links to external websites are provided as a resource to the viewer. This website is neither owned nor controlled by Pfizer Ltd.
Pfizer accepts no responsibility for the content or services of the linked site other than the information or other materials relating to Pfizer medicines or
business which it has provided or reviewed.
PP-PFE-GBR-3859. November 2021